В действительности же СзА быстро
В действительности же СзА быстро
Химия цемента - X. Тейлор
Швайзе [1031] отмечал,
что в этой системе часто трудно достичь равновесия. Одним из следствий является
тенденция ферритной фазы образовывать кристаллы с зонной структурой. Для составов
ряда Ca2(AlrFe1_r)205 отношение Al/Fe
в жидкости выше, чем в ферритной
фазе, с которой жидкость находится в равновесии. Кристаллы, которые
первоначально выпадают в осадок при охлаждении этой жидкости, имеют поэтому
более низкое значение отношения Al/Fe, чем
валовый состав смеси. При дальнейшем охлаждении отношение Al/Fe в осаждаемом материале постепенно повышается. Трудно
добиться равновесия внутри ферритных кристаллов, поэтому их структура остается
зонной, причем ядро обогащено Fe3+, а наружные области содержат больше А13+, по сравнению со средним
составом.
В отечественной литературе „алюмоферритных“ — Прим. перев.
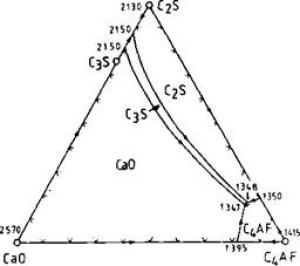
Рис. 2.6. Система СаО — СгЭ — С4АГ, по данным Ли и
Паркера [660] с последующими уточнениями.
Другим следствием
является тенденция к образованию защищенных фаз. Если охладить жидкость,
состав которой соответствует несколько более богатой оксидом кальция стороне
пограничной кривой между СаО и первичным фазовым полем СзА (рис. 2.5), то
вначале в осадок выпадает оксид кальция, и состав жидкости движется от СаО по
направлению к этой пограничной кривой. По достижении этой границы, при условии,
что поддерживается равновесие, оксид кальция должен был бы вновь раствориться,
СзА — выпасть в осадок, а состав жидкости должен был бы двигаться вдоль
границы. В действительности же СзА быстро окружает частицы оксида кальция,
который и образует защищенную фазу, эффективно выводимую из системы. Это может
заметно влиять на состав ферритной фазы, которая обрадуется при дальнейшем
охлаждении.

 44
44