Составы ферритной фазы определяются
Составы ферритной фазы определяются
Химия цемента - X. Тейлор
<>
name=bookmark47>2.3. Системы, содержащие Ре20з
<>
name=bookmark48>2.3.1.
Система СаО — А1203 — Fe203
Эта система включает ряд ферритных1) составов Caa(AlxFei_x)i05. Одна из границ, бинарная система СаО — Fe203, включает
три соединения, а именно C2F, CF и
CF2.
C2F как конечный член
ферритного ряда, обсуждается в разд. 1.5. Другие два соединения менее важны для
химии цемента. Филлипс и Муан [893] при исследовании двойной системы нашли,
что CF плавится инконгруэнтно при 1216°С с образованием C2F и жидкости и что CF2 распадается
при 1155°С с образованием CF и
гематита (a-Fe20a). В этой и других системах, содержащих Ге20з, богатые железом смеси
имеют тенденцию терять кислород при нагревании на воздухе выше 1200-1300°С с
последующим образованием магнетита (FeaO-j) вместо
гематита.
На рис. 2.5 представлена часть тройной системы СаО —А120з — Fe203- С3А, С12А7, СА все могут размещать в своих решетках некоторое
количество Fe3+;
для С3А в равновесных условиях при 1325°С предельное содержание железа составляет
около 4,5% в пересчете на Fe203 [733].
Ферритная фаза в равновесии с железосодержащим С3А может иметь состав со значениями х от 0,48 до 0,7 в формуле
Ca2(AlrFei_r)20s; если присутствует и СаО, то х = 0,48, т. е. состав
близок к C4AF. Если ферритная фаза синтезируется из смесей ряда Ca2(AlrFei_;C)205 на воздухе, происходит частичное восстановление Fe3+ до Fe2+. Это приводит к образованию небольшого количества других фаз, которые не
наблюдаются, если подобный эксперимент проводить в кислороде [733].
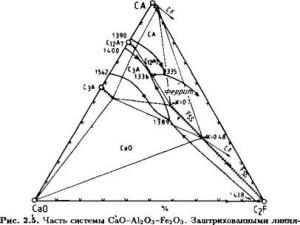
ми обозначены твердые растворы. Составы ферритной фазы определяются
значением х в формуле Са2(А1*Ееі_і)2С>5.
По данным [733, 846].

 43
43