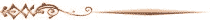Система СаО 2 По
Система СаО 2 По
Химия цемента - X. Тейлор
•V

Рис. 2.9. Система СаО — C2S — CaFî- По данным Гатта и Осборна [402] (Building
Research Establishment, Crown Copyright).
Вторая тройная фаза описывалась как ЗСзБ • СаР2 [390], Сц84 • СаГ2 [1155] и СхэБу • 2СаР2 [401]; но, вероятно, ее формула Саб^/г^гОю-гГ* (х ~ 1). Структура этой фазы родственна структуре СзБ, в которой О-2 частично замещены на Г-, и это сбалансировано потерей Са2+
[900, 901]. Расположение ионов Са2,8104” и О2- или Г- отличается от расположения в полиморфных
модификациях СзБ и является, по-видимому, наипростейшим среди обширного
семейства структур, которыми может обладать Сзв [900]. Имеется строго
определенная псевдоячейка, являющаяся (при х = 1,0) гексагональной с
параметрами а = 0,7099 нм, с = 0,5687 нм; пространственная группа
Рбз/ттс, атомный состав 1/2[Ою84 • СаГг]. Но истинная ячейка — триклинная, с параметрами
а = 2,3839 нм, Ь = 0,7105 нм, с = 1,6755
нм, а = 90,0°, /3 = 117,3°, 7 = 98,56°, атомный состав 5[Сю84 • СаР2] [900, 901]. Рентгеновская плотность для х = 1,0 равняется 2936 кг/м3. Для краткости мы будем называть эту
фазу Ск^ • СаР2.
В системе СгЭ — СаР2 два конечных члена образуют эвтектику при 1110°С. 2С28
• СаР2 может быть получен твердофазной реакцией при 950° и
распадается при 1040°С с образованием С2& и Сар2 [400]. Результаты двух исследований фазовых равновесий в системе СаО—СгБ—СаГ2 [402,1155] (рис. 2.9) хорошо согласуются.
CioS4 -CaF2 плавится
инкогруэнтно при 1170°C с образованием C3S и жидкости. Таким образом в присутствии CaF2 C3S можно
получить при этой температуре путем последовательного образования и распада
при более низких температурах соединений 2C2S • CaF2 и C10S4 •
CaF2 [56, 403, 1155].
Есть некоторая неопределенность относительно того, какое количество F- может
входить в структуру C3S (в
противоположность C10S4 • CaF2), а также относительно эффективности C3S, полученного в присутствии CaF2, как цемента. Уэлч и Гатт [1254] нашли, что добавка CaF2 к
исходным материалам влечет за собой превращение триклинной модификации в
моноклинную, и получили данные, позволяющие предположить, что в структуру C3S входит 0,74% F- ;
CaF2 ускоряет
образование C3S, но понижает прочность на сжатие. Танака и др. [1155] нашли, что C3S, образующийся из C10S4 • CaF2, имел тригональную структуру (по-видимому,
ромбоэдрическую), хотя она имела тенденцию к превращению в моноклинную при
закалке. Они нашли, что C10S4 CaF2 дает низкие прочности, и считали, что слабая
гидравлическая активность препаратов Уэлча и Гатта была, возможно, связана с
присутствием этой фазы, полученной из C3S при
охлаждении. Маки и др.

 56
56