2.2.6. Образование клинкера в системе СаО — А^Оз — ЗЮг
2.2.6. Образование клинкера в системе СаО — А^Оз — ЗЮг
Химия цемента - X. Тейлор
Известны несколько других безводных алюмосиликатов кальция, включая
гроссуляр или гранат (C3AS3) —
фазу, которая получается при высоком давлении, а также различные продукты
дегидратации цеолитов и продукты, образующиеся метастабиль-
но при кристаллизации из
расплавов или стекол. Большая часть этих соединений слишком кислотная по
составу, чтобы иметь прямое отношение к химии цемента, но некоторые продукты
девитри- фикации, особенно те, что имеют составы, близкие к СА, и структуры,
сходные со структурами нефелина ЙазКАЦБЦОхб или каль- силита КА1БЮ4 [1286], возможно, представляют интерес в связи с
образованием кальциевоалюминатных цементов.
2.2.6.
Образование
клинкера в системе СаО — А^Оз — ЗЮг
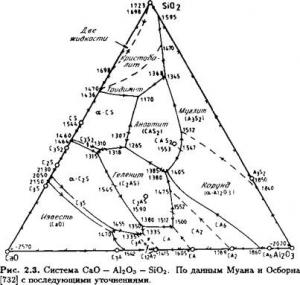
Диаграмма системы СаО — АЬОз — БЮ? дает базис для предварительного
понимания химических процессов, лежащих в основе образования
портландцементного клинкера; все, кроме трех наиболее важных оксидных
компонентов, в этом случае опущены. В меньшей степени эта диаграмма пригодна
для белых цементов. Максимальна^ температура, достигаемая смесью в цементной
печи, которая называется температурой клинкерообразования, обычно равна
1400-1450°С; при этой температуре смесь частично плавится. Чтобы смесь в
чистой системе СаО — А1203 — ЭЮг достигла сравнимого состояния, требуется
несколько более высокая температура. В этом обсуждении мы будем предполагать,
что равновесие достигается при температуре клинкерообразования 1500°С, и
использовать диаграмму СаО — А1203 — 8Ю2 для предсказания того, какие твердые фазы будут
присутствовать в композициях с различным химическим составом. Реакции, при
помощи которых процесс получения цемента приближается к равновесию, и процессы,
имеющие место при последующем охлаждении, обсуждаются в гл. 3.

 40
40